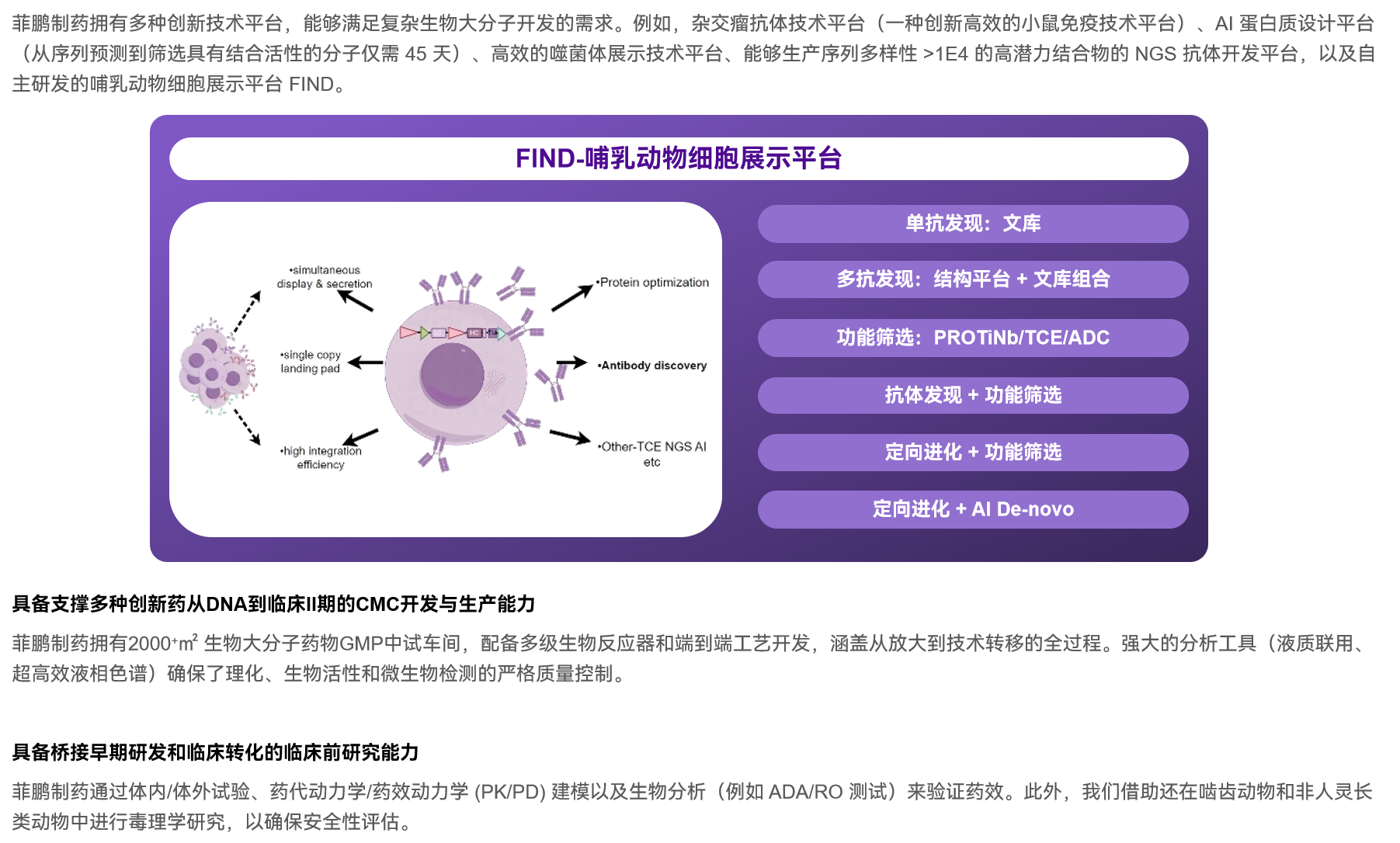
菲鹏创新与差异化的抗体技术平台
以解决现有技术和产品不足为目标,开发创新、差异化和普适应创新技术
细胞因子融合抗体平台(FILTEN)
FILTEN解决了IL-10的局限性,在肿瘤和自身免疫性疾病中拥有极大的拓展空间
-解决了野生型IL-10半衰期短和血液毒性强的局限性
-双功能分子展现出更强的药效
-在肿瘤和自身免疫性疾病中拥有极大的拓展空间
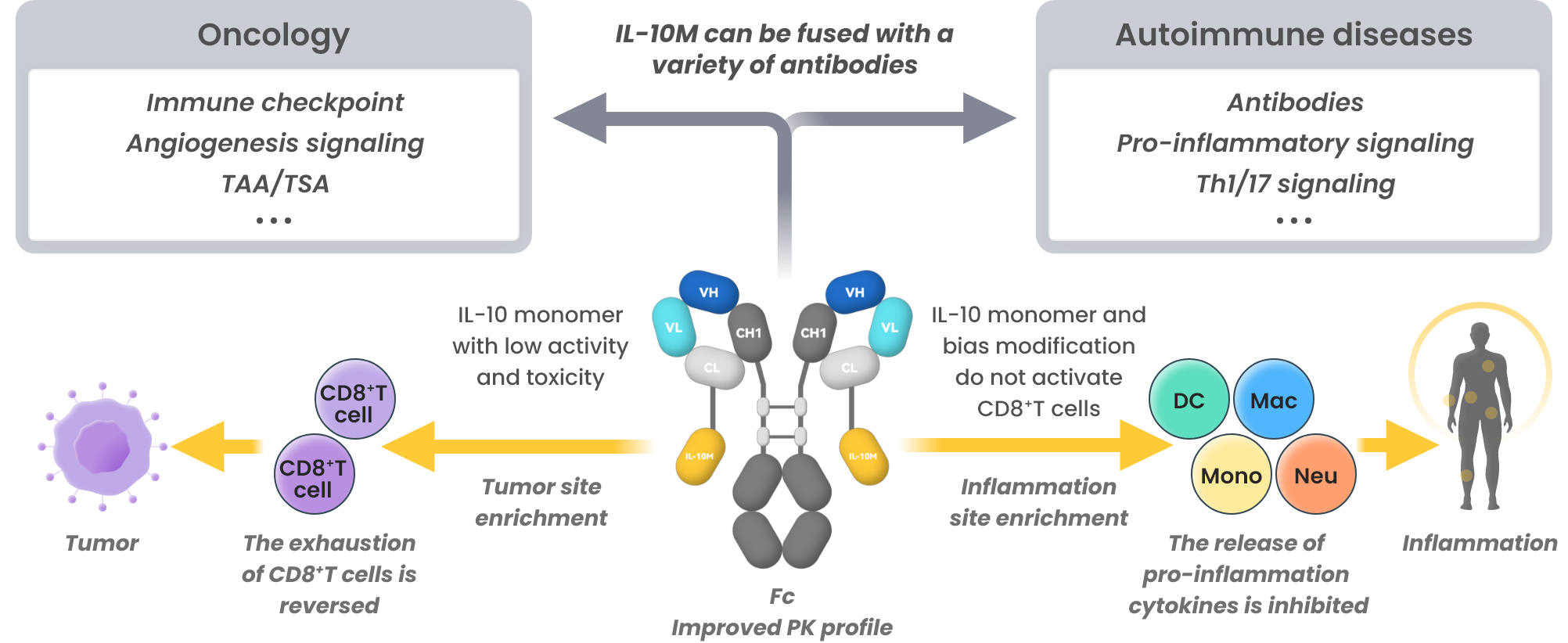
(注:TAA = 肿瘤相关抗原;TSA = 肿瘤特异性抗原;PK = 药物代谢动力学;DC = 树突细胞;Mac = 巨噬细胞;Mono = 单核细胞;Neu = 嗜中性粒细)
双/三抗TCE平台
TCE平台拥有多种高质量、差异化核心组件和结构
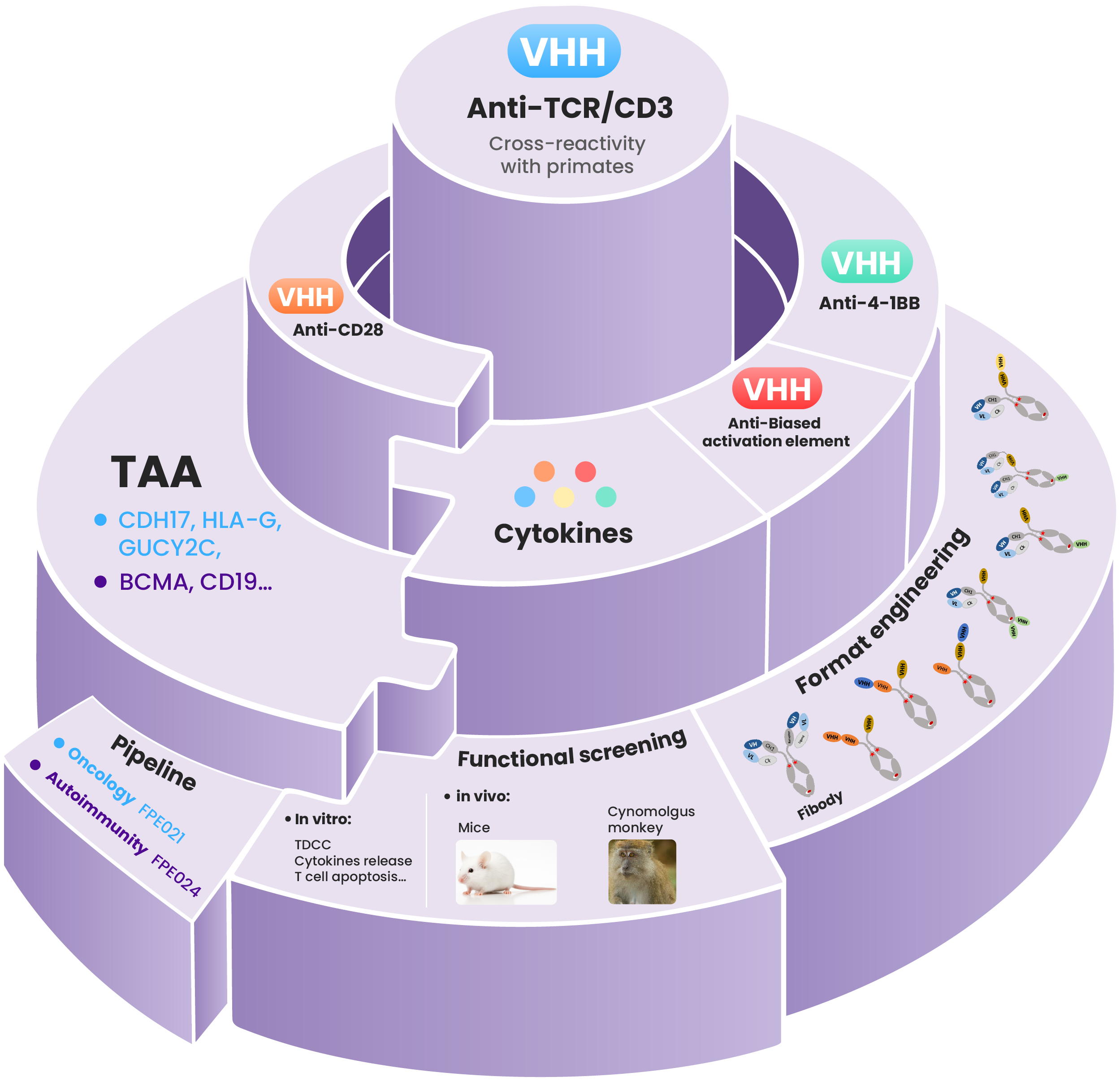
纳米抗体优势:
拥有呈现猴交叉反应活性的抗 TCR/CD3 纳米抗体,以及具备适配活性的共刺激(第二信号)纳米抗体,可充分满足复杂分子结构设计中的多样化选择需求。
精研TCE管线:
多条管线协同推进,重点开发三代TCE、CD8T偏向性TCE以及能够解决TCE耐药问题的TCE等。
序列多元赋能:
开发的不同活性的核心组件序列满足内部开发与对外授权需求。
PROTiNb平台
PROTiNb平台可靶向不可成药胞内靶点:更安全、更高效、拓展性更好
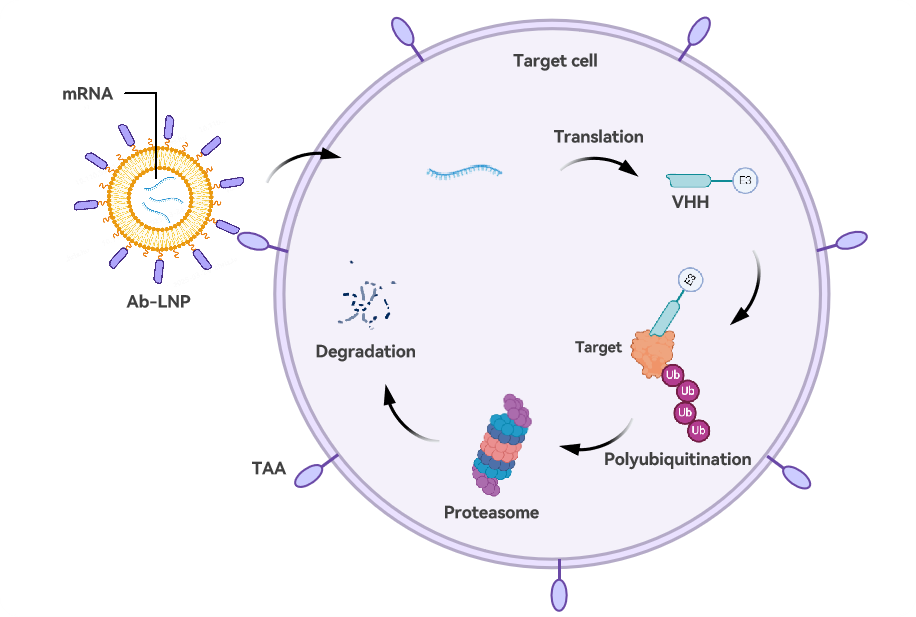
PROTiNb平台介绍:
以靶向LNP为递送载体,递送降解分子mRNA至靶细胞内,进一步翻译成效应蛋白:包括靶向目的蛋白的VHH、linker和启动泛素化降解的E3组件,最终目的蛋白被特异性降解,以改变靶细胞特性。
PROTiNb平台优势:
-靶向不可成药胞内靶点
-通过VHH抗体靶向,高效、特异、安全
-E3酶选择性广泛,不受特定E3表达分布影响
-效应分子2端亲和力可改造,应用更广泛
抗体技术平台